Le sepsis reste l’un des défis les plus redoutables de la médecine moderne. Il ne s’agit pas simplement d’une infection, mais d’une défaillance systémique catastrophique dans laquelle la réponse immunitaire de l’organisme se retourne contre elle-même, attaquant les tissus et organes sains. Même avec des traitements avancés pour l’infection sous-jacente, les taux de mortalité restent stupéfiants : environ 32 % des patients atteints de sepsis décèdent dans les 90 jours, un chiffre qui grimpe à 39 % pour ceux qui entrent en choc septique.
Cependant, une nouvelle approche thérapeutique, ciblant une protéine spécifique responsable de cette spirale hyper-inflammatoire, s’est révélée très prometteuse dans des études récentes.
Le coupable : Galectine-3
Depuis des décennies, les chercheurs étudient une protéine connue sous le nom de galectine-3. Dans un corps sain, cette protéine joue un rôle essentiel dans la régulation de la croissance, de la division et de l’activation des cellules immunitaires. En raison de sa nature polyvalente, il a été associé à diverses affections, allant du cancer aux maladies auto-immunes.
L’idée révolutionnaire, défendue par Isaac Eliaz de la clinique médicale et centre de guérison Amitabha, consistait à déterminer si la galectine-3 agissait comme le principal moteur de l’inflammation mortelle observée dans le sepsis. Cette hypothèse a gagné du terrain après que des études ont révélé une tendance constante : des taux plus élevés de galectine-3 dans le sang sont étroitement corrélés à des taux de mortalité plus élevés chez les patients atteints de sepsis.
Une nouvelle méthode de traitement : la filtration du sang
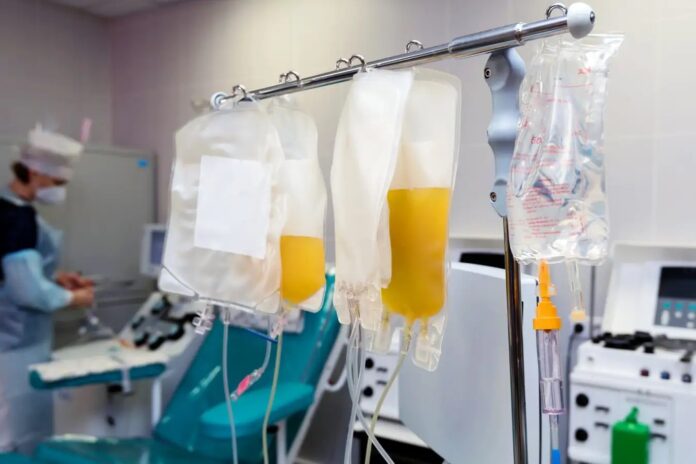
Plutôt que d’utiliser des médicaments traditionnels pour inhiber la protéine, les chercheurs ont développé un moyen mécanique de l’éliminer physiquement de la circulation sanguine. Ce processus, appelé aphérèse, se déroule en plusieurs étapes précises :
- Extraction : Un volume de sang est prélevé sur le patient.
- Séparation : Une centrifugeuse sépare le sang en cellules et en plasma liquide.
- Filtration sélective : Le plasma passe à travers un filtre spécialisé contenant des anticorps spécialement conçus pour capturer la galectine-3.
- Réintégration : Le plasma purifié et les cellules du patient sont recombinés et renvoyés dans l’organisme.
Preuves du laboratoire : la réussite des animaux
Pour valider cette technologie, une équipe de recherche dirigée par Zhiyong Peng de l’hôpital Zhongnan de l’université de Wuhan a mené une série de tests rigoureux. Leurs résultats suggèrent que la suppression de la galectine-3 pourrait augmenter considérablement les taux de survie.
Principaux résultats de la recherche :
- Corrélation humaine : Dans une étude portant sur 87 patients atteints de sepsis, les chercheurs ont confirmé que ceux qui en étaient atteints présentaient des taux de galectine-3 significativement plus élevés, qui ont ensuite chuté chez les patients qui ont survécu.
- Modèles de rats : Dans les expériences où des rats ont été induits en septicémie, ceux traités avec le dispositif de filtration avaient un taux de survie de 57 %, contre seulement 25 % dans le groupe témoin.
- Modèles de cochons : Dans des modèles de cochons miniatures plus complexes, les résultats étaient encore plus frappants. Malgré des soins intensifs standards, les porcs traités par aphérèse à la galectine-3 ont enregistré un taux de survie de 69 %, tandis que le groupe témoin n’a enregistré que 27 %.
Le chemin vers l’utilisation clinique
Même si ces résultats sont très encourageants, la communauté médicale reste prudemment optimiste. Des experts, dont Djillali Annane de l’hôpital Raymond Poincaré, notent que même si l’innovation est importante, plusieurs obstacles subsistent.
Avant que cela ne devienne un traitement standard au chevet du patient, les scientifiques doivent :
– Comprendre pleinement les mécanismes biologiques exacts par lesquels la galectine-3 provoque la septicémie.
– Reproduire ces résultats dans des études indépendantes.
– Tester l’efficacité chez des animaux d’ordre supérieur, tels que les primates, pour mieux imiter la physiologie humaine.
“Les résultats sont cohérents dans les deux modèles animaux”, note Annane, tout en soulignant le long chemin à parcourir pour une standardisation.
Regarder vers l’avenir
La transition du succès du laboratoire à la réalité hospitalière est une entreprise colossale. Eliaz Therapeutics recherche actuellement les financements nécessaires pour lancer des essais cliniques randomisés chez l’homme, provisoirement ciblés pour 2027.
Conclusion
En cas de succès dans les essais sur l’homme, l’aphérèse de la galectine-3 pourrait transformer le traitement du sepsis de la gestion des symptômes à la neutralisation active du moteur biologique de la défaillance d’un organe. Ce changement pourrait potentiellement sauver des millions de vies en stoppant la progression du choc septique avant qu’il ne devienne mortel.