Wissenschaftler haben einen epigenetischen Schlüsselmechanismus identifiziert, der die Entwicklung von Fettzellen steuert und einen potenziellen neuen Weg zur Behandlung von Fettleibigkeit und damit verbundenen Stoffwechselstörungen eröffnet. Die am Korea Advanced Institute of Science and Technology durchgeführte Forschung beschreibt detailliert, wie ein Signalweg den primären Treiber der Fettzellenbildung, das PPARγ-Protein, außer Kraft setzen kann.
Die Rolle von PPARγ bei der Entwicklung von Fettzellen
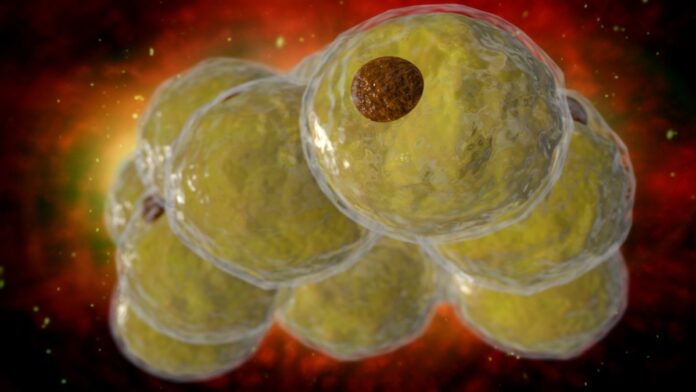
PPARγ ist als „Hauptregulator“ der Adipogenese bekannt – dem Prozess, durch den Zellen zu Fettzellen (Adipozyten) werden. Wenn PPARγ aktiv ist, löst es eine Kaskade genetischer Veränderungen aus, die eine Zelle dazu bringen, eine Fettzelle zu werden und zu bleiben. Die Blockierung dieses Prozesses ist ein Hauptaugenmerk bei der Vorbeugung von Fettleibigkeit und Typ-2-Diabetes.
Der Hippo-YAP/TAZ-Weg als epigenetische Überschreibung
Die Studie zeigt, dass der Hippo-Signalweg, insbesondere über seine nachgeschalteten Effektoren YAP und TAZ, als epigenetischer Schalter fungiert, der die Fettproduktionsanweisungen von PPARγ wirksam blockieren kann. Dies bedeutet, dass der Signalweg das Zellschicksal steuert, ohne die zugrunde liegende DNA-Sequenz zu verändern.
Warum das wichtig ist: Frühere Untersuchungen zeigten, dass YAP und TAZ die Bildung von Fettzellen beeinträchtigen, aber das wie blieb unklar. Diese Studie liefert eine mechanistische Erklärung und zeigt, wie diese Proteine PPARγ-aktivierte Gene über eine chemische Kettenreaktion deaktivieren. Dies ist von Bedeutung, da epigenetische Kontrollen oft formbarer sind als genetische und möglicherweise neue therapeutische Fenster eröffnen.
Blockierung der „Bremsen“ der Fettzellenproduktion
Forscher testeten die Wirkung der Deaktivierung des Hippo-Signalwegs bei Mäusen, wodurch die „Bremsen“ der YAP- und TAZ-Aktivität effektiv beseitigt wurden. Diese Hyperaktivierung führte dazu, dass sich vorhandene Fettzellen zurückbildeten, ihre charakteristischen Eigenschaften verloren und in einen eher Vorläufer-ähnlichen Zustand zurückkehrten.
Wichtiges Ergebnis: Die Studie zeigt, dass die Differenzierung von Fettzellen auf epigenetischer Ebene präzise gesteuert wird und über die einfache Genregulation hinausgeht. Obwohl die Forschung an Mäusen durchgeführt wurde, sind die Auswirkungen auf die Stoffwechselgesundheit des Menschen erheblich.
Implikationen für die Behandlung von Stoffwechselerkrankungen
Die Fähigkeit, die Produktion von Fettzellen zu manipulieren, könnte tiefgreifende Auswirkungen auf die Behandlung von Fettleibigkeit und verwandten Erkrankungen haben. Im Gegensatz zum Schrumpfen der Fettzellen beim Abnehmen deutet dieser Mechanismus darauf hin, dass ihre Entstehung überhaupt erst verhindert werden kann.
Zukünftige Richtungen: Obwohl die Ergebnisse vielversprechend sind, sind weitere Forschungsarbeiten erforderlich, um diese Entdeckungen in sichere und wirksame Therapien für den Menschen umzusetzen. Die Studie legt eine entscheidende Grundlage für das Verständnis von Veränderungen der Adipozytenidentität und letztendlich für die Entwicklung personalisierter Behandlungsstrategien für Stoffwechselerkrankungen.
„Diese Studie hat eine wichtige Grundlage für ein tieferes Verständnis der Mechanismen hinter Adipozyten-Identitätsveränderungen und langfristig für die Entwicklung personalisierter Behandlungsstrategien für Patienten mit Stoffwechselerkrankungen gelegt“, schließt der Molekularbiologe Dae-Sik Lim.